第三节 清道夫受体
遗传性的LDL受体缺陷的杂合子是不能摄取LDL的,但动脉粥样硬化斑块的巨噬细胞有从LDL来的胆固醇酯大量蓄积并泡沫化,其原因用LDL受体途径无法解释,因为从这条途径不能摄取对过多的脂质。同时经LDL受体摄入脂类的量是受细胞内胆固醇水平的调节。Brown与Goldstein等使LDL乙酰化,从而导致不受细胞内胆固醇调节的过剩脂质也摄入并出现异常蓄积,进而推测存在一种LDL受体途径以外的脂质摄取途径,使巨噬细胞摄取乙酰化LDL。Brown等人提出这种设想并定名为清道夫受体(scarenger receptor)。以后许多实验证明了这种推测。1984年Heinecke等人在细胞培养液中添加氧化剂使LDL氧化修饰,其结果使巨噬细胞摄取了这种变性LDL。现在认为,人体内脂质过氧化反应导致的变性LDL,可被巨噬细胞无限制地摄人细胞内,这是因为变性LDL上带有各种分子的负电荷而与清道夫受体结合。
一、清道夫受体结构Komada等于1990年用配体亲和层析和免疫亲和层析,将牛肺巨噬细胞清道夫受体纯化,并由其部分氨基酸序列(见图6-7)克隆得到Ⅰ型、Ⅱ型清道夫受体cDNA,以后相继将人、兔和小鼠的清道夫受体cDNA克隆成功。该受体C-末端为半胱氨酸的为Ⅰ型,具有短肽结构的为Ⅱ型清道夫受体。以三聚体形式存在,分子量为22kD的膜糖蛋白。N末端在细胞膜内侧,C末端在膜外侧存在,是“inside out”型的受体。该受体的Ⅰ、Ⅱ型均由6个区域部分组成,如图6-8所示。
1.N-端胞浆域 由50个氨基酸残基组成,可能与包涵素结合,类似LDL受体结构。其中央部分是磷酸化部位,摄取配体的最重得要的部位。
2.跨膜域(transmembrane) 由第51~76氨基酸残基构成。为疏水性氨基酸组成的单一结构,“抛描”固定于细胞膜上。
3.间隔域 由第77~150氨基酸残基构成。
4.α-螺旋卷曲螺旋域(α-hericalcoiled-coil)由第151~271共121个氨基酸残基组成。在这段蛋白中,其中含糖基结构域中有7个氨基酸残基组成的一含疏水性氨基酸的高氨酸拉链(leucine-zipper-helix)结构或者称为“七联体”,如图6-9所示,这种结构可以多达23个。

图6-7 清道夫受体氨基酸序列比较

图6-8 清道夫受体结构模式图
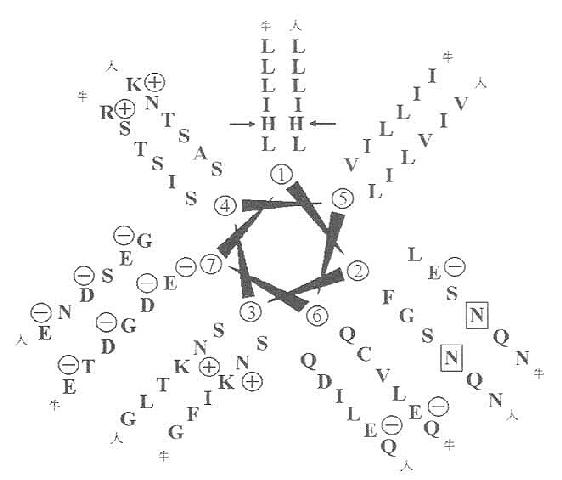
图1-9 清道夫受体的亮氨酸拉链结构
图中为α-螺旋卷曲螺旋域中的螺旋轮示意图(人与牛)
亮氨酸拉链结构的肽段先叠成右手α-螺旋,每一圈含3.5个氨基酸。尔后这些α-螺旋以疏水氨基酸中心构成的平行的三聚体结构。该结构域内,亮氨酸与异亮氨酸残基出现部分对人则是分别为155~203和240~272氨基酸残位置。
5.胶原蛋白样域 属第273-343个氨基酸残基肽段,这种序列与胶原蛋白非常相似,推测这段肽链为右手胶原蛋白样三联体螺旋。
6.C端侧特异域 属第344~453个氨基酸残基肽段,为羧基末端。该段富含半胱氨酸。清道夫受体的8个Cys有6个在此域范围,所以称为清道夫受体富半胱氨酸域(scavenger receptor cystein rich domain like, srcR域)。半胱氨酸的二硫键交联而成的区域非常紧密,牢固,形成球状,足以经受细胞外环境的变动,属于细胞外区域。
srcR域长约430nm,犹如三朵郁金香的“花苞”,有由间隔域到α-螺旋卷曲螺旋域构成的“花茎”为支撑,这一“花茎”约占总长度的52%或胞外部分的62%。Ⅱ型清道夫受体没有srcR域,代之以6个氨基酸残基,所以是“截短”的清道夫受体。但Ⅱ型清道夫受体比Ⅰ型清道夫受体具有高亲和力结合和介导内移修饰LDL作用。
二、清道夫受体配体清道夫受体配体广泛,有:①乙酰化或氧化LDL等修饰的LDL;②多聚次黄嘌呤核苷酸和多聚鸟嘌呤核苷;③多糖如硫酸右旋糖酐;④某些磷脂,如丝氨酸磷脂,但卵磷脂不是配体;⑤细菌脂多糖,如内毒素等。这样广泛的配体谱的共同特点是多阴离子化合物。Ⅱ型清道夫受体没有srcR域,但仍具有Ⅰ型相同的功能,显然配体结合域不在srcR域,推测其结构域在胶原蛋白样域C末端的22个氨基酸残基作为配体识别位点。是结合多阴离子配体所必需的位点。
三、清道夫受体功能目前对于清道夫受体的功能还不十分清楚,是人们在研究巨噬细胞转变成泡沫细胞的机制时发现的。近年来大量实验证明LDL可被巨噬细胞、血管内皮细胞和平滑肌细胞氧化成氧化LDL,可通过清道夫受体被巨噬细胞摄取,形成泡沫细胞,氧化LDL还能吸引血单核细胞粘附于血管壁,对内皮细胞有毒性作用等,从而促进粥样斑块形成。这些研究无疑阐明了巨噬细胞的清道夫受体在粥样斑块形成机制中起有重要的作用,另一方面,也推测巨噬细胞通过清道夫受体清除细胞外液中的修饰LDL,尤其是氧化的LDL,是机体的一种防御功能。可清除血管壁过多脂质;清除病菌毒素,摄取内毒素多方面的功能。
清道夫受体分布于胎盘,肝脏、脾脏等网状内皮系统,脑组织也有Ⅰ型和Ⅱ型。
清道夫受体不仅在组织巨噬细胞内发现有,在单核细胞分化由来的巨噬细胞侵入内皮的过程中也见有该受体。兔、大鼠高脂肪膳食模型制作过程中,喂饲高胆固醇开始的的几天见到LDL样粒子附着于血管壁,其后有单核细胞附着于内膜、巨噬细胞导致脂肪线条病巢形成并出现成百成千巨噬细胞簇出现,此时发现有大量的清道夫受体,病灶逐步进入平滑肌细胞内膜,然而其深部巨噬细胞仅有少量残存受体,其量也逐渐减少。当变性LDL显著增加时,清道夫受体摄取的脂质则不受制约,目前认为这是脂质沉积的重要原因,也是动脉粥样硬化发病的重要机制。使LDL变性的主要因素是脂质的过氧化,而何种原因引起脂质过氧的,有待进一步研究。
(周新)
