第一节 载脂蛋白分离纯化
一、分离脂蛋白
血浆是分离纯化脂蛋白的首选标本。从血浆(血清)中可分离得到CM、VLDL、LDL和HDL,再经脱脂除去脂蛋白中的脂质,剩下的部分为载脂蛋白的混合物。这一操作过程是获得载脂蛋白的最佳方法。
二、脱脂
由于各种脂蛋白含脂的种类和质量不同,脱脂剂组成略有差异。目前常用的几种脱脂方法有如下几种。
1.Warnick等法
将纯化的脂蛋白慢慢加入到预冷(-20℃)的丙酮:无水乙醇(1:1,V/V)混合液中,脱脂液的量为样品的20倍,不断搅拌,然后在-20℃冰箱放置过夜,4℃离心沉淀,将沉淀重复脱脂一次,用氮气吹干或真空干燥,脱脂物0℃贮存待用。
2.Scanu等法
将脂蛋白加入到预冷的(-15℃)无水乙醇:无水乙醚(3:2)混合液中,不断搅拌,以12h过夜,在-10℃或4℃离心(2000r/min),去上清留沉淀,再重复脱脂一次。用N2或真空干燥,0℃贮存待用。
三、载脂蛋白的分离纯化法
(一)凝胶过滤法
凝胶过滤(gel filtration)技术是60年代兴起的一种简便有效的生物分离纯化方法。当混合溶液通过凝胶过滤层析柱时,因凝胶具有网状结构,小分子物质能进入其内部,而大分子物质却被排阻于外部,在过滤的过程中,溶液中的物质按不同分子量筛选分开,达到分离纯化的目的。这一技术又称为分子筛层析,或者称为凝胶层析。
凝胶是不溶于水,在水中却有较大膨胀度和较好的分子筛功能的一类化合物。目前主要有葡聚糖凝胶(商品名为Sephadex),天然琼脂糖凝胶(商品名为Sapharose)、聚丙烯酰胺凝胶(商品名为Bio-Gel),其后还发展了凝胶的各种衍生物,如羧甲基-交联葡聚糖(CM-Sephadex),二乙基氨乙基-交联葡聚糖(DEAE- Sephadex)等种类。
由于凝胶过滤技术设备简单、操作方便,重复性能好和样品得率高等特点。广泛应用于生命科学领域,如蛋白质、核酸、多糖氨基酸、激素和抗生素等物质的分离纯化。凝胶层析在载脂蛋白的分离纯化中,属于使用最多的技术手段。
凝胶过滤装置种类很多,其基本操作过程大同小异,操作步骤主要有:①凝胶种类的选择,按被分离物的性质及分子量大小而定;②凝胶柱的制备;③加样与洗脱;④分部收集透析,浓缩。
载脂蛋白分离纯化,多采用SephadexG-200层析分离。
1.ApoAⅠ、AⅡ的凝胶过滤分离纯化法:①超速离心获得HDL,以醇:醚(1:1)脱脂,-10℃脱脂6~8h,离心,弃上清留沉淀;②以6mol/L尿素Tris-HCl缓冲液(0.1mol/L,pH8.5)溶解沉淀;③加样于SephadexG200凝胶柱。以6mol/L尿素Tris-HCl缓冲液(0.1mol/L,pH8.5)洗脱;④洗脱液经紫外监测仪(280nm)监测后,由部分收集器按吸收峰分部收集;⑤对各组份进行鉴定,收集需要的蛋白峰,透析,浓缩。
2.ApoE、CⅡ、CⅢ的凝胶过滤分离纯化法:
ApoE、CⅡ、CⅢ均以VLDL为材料,与ApoAⅠ类同的方法进行凝胶层析分离。
(二)亲和层析法
亲和层析是60年代末发展起来的一项分离纯化技术,目前已得到广泛的应用。亲和层析的原理与抗原对抗体、激素对受体和酶对底物等特异性反应的机理类同,每对反应物之间都有一定的亲和力。亲和层析是把被识别的分子(底物、配体或抗原)以共价键结合到含有活化基团的固相载体例如琼脂糖珠上,然后使含有欲分离的大分子化合物的混合液从这个载体滤过,极大部分对配体没有亲和力的化合物,均顺利通过载体而不滞留,欲分离的大分子能识别配体(有亲和力)并与其结合,而滞留在层析柱上,等所有杂质从层析柆上流走后即第一个层析峰出现后,改变洗脱条件,促使结合在配基上的大分子化合物解离下来并形成了第二个层析峰,原来混合液中欲分离的大分子化合物则以高度纯化的形式在流出液中出现,得到需要分离纯化的物质。亲和层析法几乎适用任何可以纯化的大分子化合物,如酶、抗体、抗原、激素、药物、核酸、维生素结合蛋白质,转运蛋白、阻抑蛋白、载脂蛋白和其他调控成分等。
亲和层析操作过程简述如下。
1.载体的选择
选择亲和层析所用的载体必须符合的条件有:①非特异性吸附要低;②有良好的流动特性;③在pH离子强度和变性剂浓度较大改变的情况下,化学和机械等理化性能稳定;④具备大量能被活化的化学基因;⑤高度有效的多孔结构。实际工作中,尤其是载脂蛋白的分离纯化多用琼脂糖珠(Sepharose 4B)作为载体选用。
2.配体(配基)的选择
亲和层析应根据被分离纯化的物质的理化性质和生物学性质而选择配本,一般考虑选择的条件是;①与纯化的物质有较强的亲和力。作为载脂蛋白的纯化常常选择Apo的相应抗体作为配体;②具有与基质共价结合的基团。
3.配体与载体的联结
配体与载体共价联结的方法包括:①载体功能基团的活化;②配体与活化基团的联结。使二者进行联结的化学反应必须足够温和,使配体和载体均可耐受而不发生变性。
配体与载体的联结方法有物理和化学的两类。最常用的方法是化学法,化学法包括偶联法和交联法,又以交联法常用,常用的化学试剂溴化氰(CNBr)环氧氯丙烷,双环氧乙烯、丁二烯砜和亚氨二乙醇等,用其活化的载体与配体偶联。或者使载体与配体螯合起来进行联结。
载脂蛋白纯化的常用方法是溴化氰偶联法,其操作过程包括:①活化,取一定的贮存载体Sepharose 4B用布氏漏斗抽干,加入等量的蒸馏水,并与等量的2mol/L的Na2CO3溶液(pH11~12)混匀。另取固体CNBr50~300mg/g贮存胶溶于二甲基甲酰胺溶液中,随后迅速加到搅拌的Sepharose 4B悬浮液内进行活化,其pH始终保持11~12范围。反应过程中因为放热,故要用碎冰置于反应杯周围控制温度在20℃左右,维持8~10min后再加碎冰,使其反应物温度制冷至4℃或更低的温度。由于活化的Sepharose 4B破坏迅速,他的半寿期在4℃约为15min,故整个操作过程必须迅速进行,以期尽快完成。将活化的Sepharose 4B反应液迅速转到布氏漏斗中,用10~20倍凝胶体积的预冷水及0.07mol/L溶液(pH8.3)洗涤。②偶联,经活化的洗涤过的载体与等体积的0.20~025mol/L碳酸盐缓冲液(含0.5mol/l NaCl)混合,每ml约含配体如抗人ApoB100-IgG100μg溶液(pH8~10)混合,缓慢搅拌2h(室温)或4℃搅拌过夜,使载体与配体充分偶联而形成固相载体。偶联后在溶液中加入Tris-HCl溶液(pH8.0),静置2h,室温下洗涤以除去过剩的配体(抗人ApoB100-IgG);③配体结合量的测定:配体结合量一般以每毫升或每克贮存胶偶联配体的量表示,其数值可用作决定亲和吸附剂实际用量的参数采用直接测定法或间接测定法测定结合量;④亲和层析:将制备好的吸附剂CNBr-Sepharose-4B-配体(抗人ApoB100-IgG)悬浮于平衡缓冲液中,然后加到装有平衡缓冲液的垂直层析柱中,待形成层析床后,以缓冲液平衡层析柱,再将混合组份的样品上柱,经一定时间后,让亲和物与固相上的配体亲和结合,尔后用一定盐浓度的缓冲液洗去无亲和力的无关组份。再洗脱结合的相亲和物,因亲和物与配体的结合虽然是非共价键结合。但比较牢固,一般缓冲液不能使其分开,此时必须在洗脱液中加入一定浓度的特殊化合物,一般采用破坏配体亲和物结合键的化合物如用3mol/l NaCl或3mol/L的硫氰酸盐或pH2~3的缓冲液可破坏抗原和抗体之间的结合,使抗原与固相抗体(或抗体与固相抗原)分离。若采用这一方法应立即除去硫氰酸盐或中和pH值等。
亲和层析柱可反复使用,一次使用后,必须将结合于固相载体上的亲和物全部洗脱干净,一般采用上述相同的洗脱液进行,再采用高浓度的中性盐溶液如0.5mol/l NaCl充分洗脱非特异性吸附于配体上的杂质,洗脱用缓冲液充分洗涤达到平衡后方可再度使用。在两次间隔期,如果时间较长,可加入柳硫汞或叠氮,钠等防腐剂以免细菌污染。
(三)聚丙烯酰胺凝胶电泳分离纯化法
电泳技术广泛应用于生命科学的领域里。在载脂蛋白的分离纯化中,电泳分离技术也是一种常被采用的方法。
因支持物的不同,电泳技术的种类有很多,本章着重介绍聚丙烯酰胺凝胶电泳技术有关的操作。
1.SDS-PAGE连续电泳洗脱分离纯化法
利用SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE),在规定时间内,混合液中的各种蛋白按分子量大小依次停留在凝胶的不同位置。再经染色脱色,即可见到多种蛋白区带,这是作为鉴定的SDS-PAGE法。如果SDS-PAGE不停地进行,含有多种蛋白混合液中的蛋白质会按小分子到大分子的顺序,使蛋白质进入阳极电极液中,若能设法分部收集从凝胶中电泳出来的各种蛋白质即可达到分离纯蛋白质的目的。
BIO-RAD公司推出一种聚丙烯酰胺凝胶电泳分离蛋白质或核酸的装置,如图17-1所示。该仪器利用连续洗脱电泳技术原理设计。电泳期间,蛋白质或核酸在电场中,迁移到凝胶基质,他们被分成环形的区带,各个区带依次迁移到凝胶底部,然后直接进入洗脱室,洗脱室由聚乙烯材料组成,并贴有透析膜,下面再衬以支持网。在蠕动泵推动下,洗脱液呈辐射状流入位于冷却柱中心的洗脱管中,经紫外监测后流入分部收集器。按吸收峰收集相应组份,即可得到被分离的蛋白质。
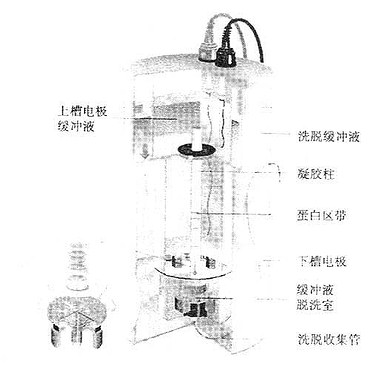
图17-1 聚丙烯酰胺凝胶电泳分离装置
为了达到分离纯化的目的,必须注意以下三方面的问题:
(1)凝胶孔径的选择:凝胶孔径主要受总浓度T%(Arc+Bis)的影响,一般是T%越大,孔径越小,其机械强度越强。当T%固定时,Bis浓度在5%时,孔径最小,高于或低于5%时,孔径都相应增大。最优分离效果的凝胶孔径必须保证其相对近移率(Rf)在0.55~0.6之间。
(2)凝胶长度的选择:适当的凝胶长度可以提高待分离蛋白质的分离效果,过长易导致蛋白区带扩散,过短则达不到分离效果。最适凝胶长度主要考虑待分离蛋白质与其相邻近的蛋白质分子量之间差异的大小(△MW),△MW与凝胶长度呈反比关系。另外还应考虑上样量的多少,适当减少上样量可达到更好的分离效果。
(3)凝胶柱大小的选择:选择凝胶柱大小主要决定于制备上样量的多少以及待分离蛋白质与其邻近蛋白△MW。Bio-RAD电泳仪有配套的28mm、3.6cm2和37mm的8.2cm2过滤柱。
(4)蛋白质电泳的洗脱时间:主要维持Rf 0.55~0.60之间,凝胶柱越长,洗脱时间越长。也可以根据实际经验选择洗脱时间。
根据作用分离制备ApoAⅠ及碱性蛋白的经验,上凝胶柱电泳前,应将血清分别作适当的处理,如分离ApoAⅠ时,在血清采用肝素锰沉淀,留下含HDL的组份;分离碱性蛋白时,先用冷乙醇处理,留下含碱性蛋白的组份。电泳分离纯化前对血清作预处理,是分离成功的关键步骤。
2.聚丙烯酰胺凝胶(PAG)切割纯化法
这一方法利用SDS-PAGE,使分离不同分子量的蛋白质,依据待分离的特定蛋白质的位置,进行切割,再捣碎其凝胶,使蛋白质析出,而达到分离纯化的目的。笔者以此方法已分离纯化了ApoBⅠ、ApoE等蛋白质。方法简便易行,缺点是回收率较低。
(四)等电聚焦分离法
等电聚焦(lsoelectro focusing ,IEF)又称为等电点分离法,是利用一种含载体两性电解质(carrier ampholyte)的凝胶在电场中形成pH梯度,同时把具有两性电解质性质的样品(如蛋白质)聚集在他们的等电点相应的pH区带中,从而达到分离蛋白质的目的。
等电聚焦,是1966年建立起来的一种高分辨率的蛋白质分子或其他两性分子的等电点的不同,在一个稳定的、连续的、线性的pH梯度载体中进行蛋白质的分离分析或纯化。
1.原理
等电聚焦技术必需的物质是两性电解质。在支持物(聚丙烯酰胺或琼脂糖)中,必须要有一个稳定的线性的pH梯度,形成这一线性pH梯度的物质就是两性载体。Rllbe早期发现谷胺酸、组氨酸和赖氨酸均能产生大约1pH的梯度,但pH范围太窄,且缓冲能力不够,因为蛋白质分子本身也是两性电解质,在电泳时,他会影响梯度pH值,为此,要求形成pH梯度的物质必须有足够的缓冲能力来克服蛋白质的影响。另外,还要求两性载体电解质必须有一个好的、均匀的导电性,使其整体系中保持电流畅通。1966年Vesterberg合成了一种两性载体物质,即由许多脂肪族的多羧基多氨基的异构体和同系物组成的混合体,利用调节胺和酸的比例可得到含氨基与羧基不同比例的脂肪族多氨基多羧基。两性电解质的pI值将在大多数羧基的pK值和大多数氨基的pK值之间,多乙烯多胺链愈长,两性电解质的pI值也越连续,即可获得平滑的pH梯度。如图17-2所示。

图17-2 平衡时载体两性电解质的浓度分布与pH梯度
两性载体必须具备下述条件:
(1)较强的缓冲能力及可溶性:聚焦过程中,为了防止蛋白质引起pH梯度的pH局部改变,保持pH梯度的稳定,两性载体必须具有较强的缓冲能力,特别是在被分离的蛋白等电点范围的缓冲作用。
(2)具有好的均匀导电性:在等电聚焦中,对等电点处必须有足够的电导,并要求各部位是均匀导电,若局部电导过小,有可能产生极大的电压降,局部发热,不仅影响pH梯度,且易使蛋白质产生热变性作用,使凝胶烧坏。
(3)两性载体本身紫外吸收值低:不与被分析的蛋白质起化学反应。
(4)无生物学效应:该物质对组织细胞及抗原的免疫性均无影响,也就是说若有少许两性电解质混入被分离的蛋白质中,并不影响其任何生物学功能。
载体两性电解质,分子量在300~1000之间,其pK和pI值各不相同但相互接近,pH范围在2.5~11之间,有pH范围不同的各类载体两性电解质,瑞典LKB公司的商品名称为“Ampholine”。
蛋白质是一种两性电解质分子,当他在大于他的等电点的pH环境中,就解离成带负电的离子,在电场中就泳动到正极;当他在小于他们的等电点的pH环境中,他变解离成带正电荷的离子,在电场中向负极泳动,这种泳动作用到达他的等电点的pH环境中,即他的净电荷为零时才停止,此时带电分子在电场作用下的迁移运动与扩散运动达到平衡。如果在一个pH梯度的环境中进行这种两性电解质(如蛋白质)的电泳,由于各种蛋白质的等电点不同,就能把不同蛋白质的分子按他们的等电点集中和分离在不同的区带中。

图17-3 蛋白质的分离模式图
箭头代表移动向,箭头长短代表移动速度,
右图为平衡时蛋白质的分离状态。
现设有等电点不同的载体两性电解质a、b、c、d、e、f混合液,在电场中泳动,pI最低(即最酸的)的a(等电点为pIa)集中在最接近阳极的部位,经浓缩缓冲后,a处于等电状态(a的实际电荷为零),这部分pH与pIa一致。仅高于a等电点的b(等电点为PIb)同样向正极电泳,但无法跨越a接近正极,与a比较,b带正电荷,仅停留在a的负极端,这一部位的pH与pIb一致。同理c停留在b的负极侧……,f在最负极端。经此电泳后,使这许多pI不同的载体两性电解质形成了从正极到负极分别为pIa-pIb-pIc-pId- pIe-pIf的pH梯度。同时这些载体两性电解质具有足够的缓冲能力,使被分离的电解质不致于影响局部的pH值。又设有不同等电点的三种蛋白质A、B、C,在两种电极液分别为酸、碱的电场中泳动,A、B、C各自向自己等电点相同的pH部分移动。使电荷消失,停止移动,即A、B、C各自停留在与pIA-pIB-pIC相同的pH部位,从而达到分离蛋白质A、B、C的目的,如图17-3所示。本方法装置简单,分辨力强,分离效果及重复性好,即可用于分离精制,也可作分析用,对标本纯度要求不严,但必须无盐存在。
在等电聚焦中,分离仅仅决定于蛋白质等电点,这是一个“稳定”过程,一旦蛋白质到达他的等电点位置,失去净电荷,该蛋白质就不能进一步迁移停留在与某一蛋白pI相同的pH值位置。等电聚点的最大优点是具有浓缩效应(或称为聚焦效应),可以对抗扩散,因此可以产生细窄稳定的蛋白区带。在这种电场中,蛋白质即使会扩散,由于是处于等电聚焦系统中,电极之间的pH梯度也是线性和连续的。如果蛋白带向阴极扩散,则将进入高pH范围而带负电荷,阳极就将吸引他回去,直到他回到净电荷是零的位置。如果他向阳极扩散,则将带正电,阴极将吸引他回到净电荷是零的位置。因此蛋白质只能在他的等电点位置被聚焦成一条窄而稳定的区带,如图17-4所示。
图17-4 IEF-PAGE图(平板电泳)
等电点分离包括三个步骤:①载体两性电解质在电场中形成pH梯度;②两性电解质(如蛋白质)经电泳分离停留在不同的pH区域;③被分离的两性电解质的鉴定和等电点(pI)的测定。
2.等电聚焦-聚丙烯酰胺圆盘电泳(IEF-PAGE)
(1)装置与仪器:
电泳仪:与聚丙烯酰胺凝胶电泳相同。
凝胶用玻璃管:5×65mm或5×120mm,作为做管状凝胶用,以下以管状凝胶为例。
(2)试剂:
| A、丙烯酰胺溶液 | (冷藏) |
| 丙烯酰胺 | 30.0g |
| 双丙烯酰胺 | 1.0g加蒸馏水至100ml |
| B、化学聚合催化溶液 | (临用时配制) |
| 过硫酸胺 | 0.35g |
| TEMED | 0.3ml加双蒸馏水至100ml |
| C、凝胶液 | (临用时配制) |
| A液 | 5ml |
| B液 | 4ml |
| 40%(W/V)两性载体 | 1ml |
| D、电极液 | 阳极:0.2%(V/V)H3PO4 |
| 阴极:4%(V/V)NaOHo | |
| E、标本溶液 | 标本(蛋白质)30~300μg和10%蔗糖约50%μl混合,可作为每凝胶管标本用量 |
以上配方可制成最终浓度为7.5%凝胶,供分子量10万以下的蛋白质如ApoAⅠ、AⅡ、AⅣ、CⅡ、CⅢ、E、H等分离纯化或鉴定使用。分子量大于10万的蛋白质可用T=3.5%~5%、C=4%~5.5%的凝胶。
(3)操作:
制胶:取C液10ml,加双蒸水10ml,混合(冷天减压排气),充填到准备好的玻璃管距离项端5~10mm高,静置待凝。
加样:将已聚合之凝胶管上层水除去,置于电泳槽内(如图17-5),2mA/管预电泳30min,上槽接

极,下槽

极,使凝胶内形成pH梯度,预电泳毕,取出凝胶管,倾去管内H3PO4液并用水洗胶面,再按图加样、电泳。
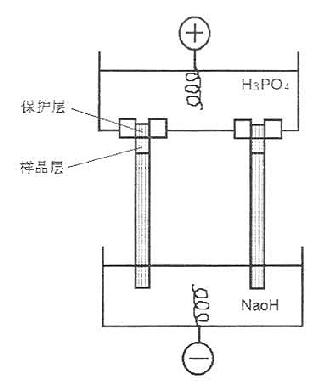
图17-5 IEF装置与标本溶液的装置(园盘电泳)
电泳:电压300~350V,2mA/管,3h,如发热,可置5℃低温环境进行,也可在200V电泳4~5h。
(4)pH梯度测定:
按聚丙烯酰胺凝胶电泳法小心推出凝胶,浸入5%TCA(10m/gel)使分离层固定,每隔1~2h换液一次,共5次,以除去载体及固定蛋白质,再按聚丙烯酰胺凝胶电泳法所述之染色,脱色。
在IEF电泳中,带两根不加标本的凝胶管,电泳毕,将凝胶剥下,按5mm之间隔切断(两根并拢同时切)分别置于0.5~1.0ml双蒸水中浸泡过夜(4℃),分别测出pH值,作图,即得pH梯度曲线。
同时电泳的加有样品的染色凝胶分别测出色带位置,从pH梯度曲线中求出该蛋白之pI。
3.等电聚焦-聚丙烯酰胺平板电泳(IEF-PAGE)
(1)仪器与试剂:
仪器 水平式电泳槽、电泳仪、有机玻璃框架、玻璃板、酸度计、光密度计。
(2)试剂:
凝胶贮存液(Acr30g、Bis0.3g,加水到100ml。)、0.35%过硫酸铵、TEMED、20%载体两性电解质(pH4~10或pH4~7)、固定液(甲醇150ml、水350ml、磺基水杨酸17.25g、三氯醋酸57.5g)、染色液(考马氏亮兰R-250约0.115g溶于100ml脱色液)、脱色液(乙醇500ml、醋酸160ml、加水到2000ml)、1m H3PO4、1M NaOH。尿素、1%琼脂糖液。
(3)操作:
制备聚丙烯酰胺凝胶等电聚焦薄板
将10.0×7.6×0.2cm的有机玻璃框架置于相应大的玻璃上,用滴管吸少量煮溶的琼脂糖液,滴入有机玻璃框架与玻璃之间、待凝。防止漏水。
制胶:以测定ApoC的PAGE-IEF为例,将下述试剂放入50ml量筒内。
| 凝胶贮存液 | 3.34ml |
| 过硫酸铵液 | 4.0ml |
| 20%载体两性电解质 | 2.0ml |
| 尿素 | 7.2g |
加蒸馏水到20ml后,搅溶尿素,再加TEMED24μl,充分混匀后,迅速倒入装置好的有机玻璃框架内,再仔细盖上一块同样大的玻璃,待凝。
预电泳:电泳槽的电极液分别为1M H3PO4(+)、1m NaOH(-),四层滤纸搭桥,160V电压下电泳40min。
加样、电泳:以0.5×0.4cm大的小滤纸片间隔1.5cm距离插入凝胶内,用微量注射器分别取待测样品(蛋白质混合液)30μl,慢慢地分别点加在各小滤纸片上,以160V电压电泳约14h。
(4)pH梯度的测定:
电泳毕,取出凝胶板,沿正极到负极方向,平等切断1cm宽的凝胶块,按0.5cm长距离从正极到负极依次切下胶带,并按顺序分别装入已编有号码(1→14)的小桡坏杯内,各加双蒸馏水1ml,振荡,静置于冰箱过夜(或2h),次日取出,平衡至室温后,用pH计测定各胶片浸出液的pH值,以每片凝胶中心位置为原点,将各胶片中心位置对相应浸出液pH值作图,即得凝胶薄板上的pH梯度曲线。
准确测量剩下的凝胶板从[

]→[

]的长度(染色前长度),再浸入固定液固定1h,尔后将凝胶置于染色液染色3~5h,再用脱色液脱色至空白胶清晰为止,此凝胶可立即用光密度计扫描积分、定量,也可以干燥后保存。
测量染色后凝胶长度,求变形系数
变形系数=染色前胶长度/染色后胶长度
再量取凝胶正极端到染色区带的距离,乘以变形系数,就等于染色区带在染色前凝胶上相应的位置。据此,可从pH梯度曲线上查出蛋白的等电点。pH梯度曲线如图17-6所示。
例如:染色前胶长(从

到

极)为7.0cm
染色后胶长(从+到-极)为7.8cm
变形系数=7.0/7.8=0.9
凝胶上的染色区带(蛋白质)到正极的距离为1.5cm
0.9×1.5=1.35
以1.35为横轴的数字查pH梯度曲线相当于pH4.8,此为该蛋白质的电点,即pI=4.8。

图17-6 IEF-PAGE的pH标准曲线图
4.载脂蛋白的纯化
等电聚焦技术对蛋白质的分辨率很高,若要用作纯品制备,可采用IEF-PAGE平板电泳。电泳完毕,从凝胶块正中或边缘切一小条(约0.3cm宽)先染色,确认待测纯品的区带位置,再将未染色的凝胶蛋白区带切下捣碎、浸泡,浸泡液中即可得到蛋白纯品。用IEF纯化蛋白质,一定要在电泳之前先处理一次得到粗制品,再行电泳。该法成本较高,得率较低。
